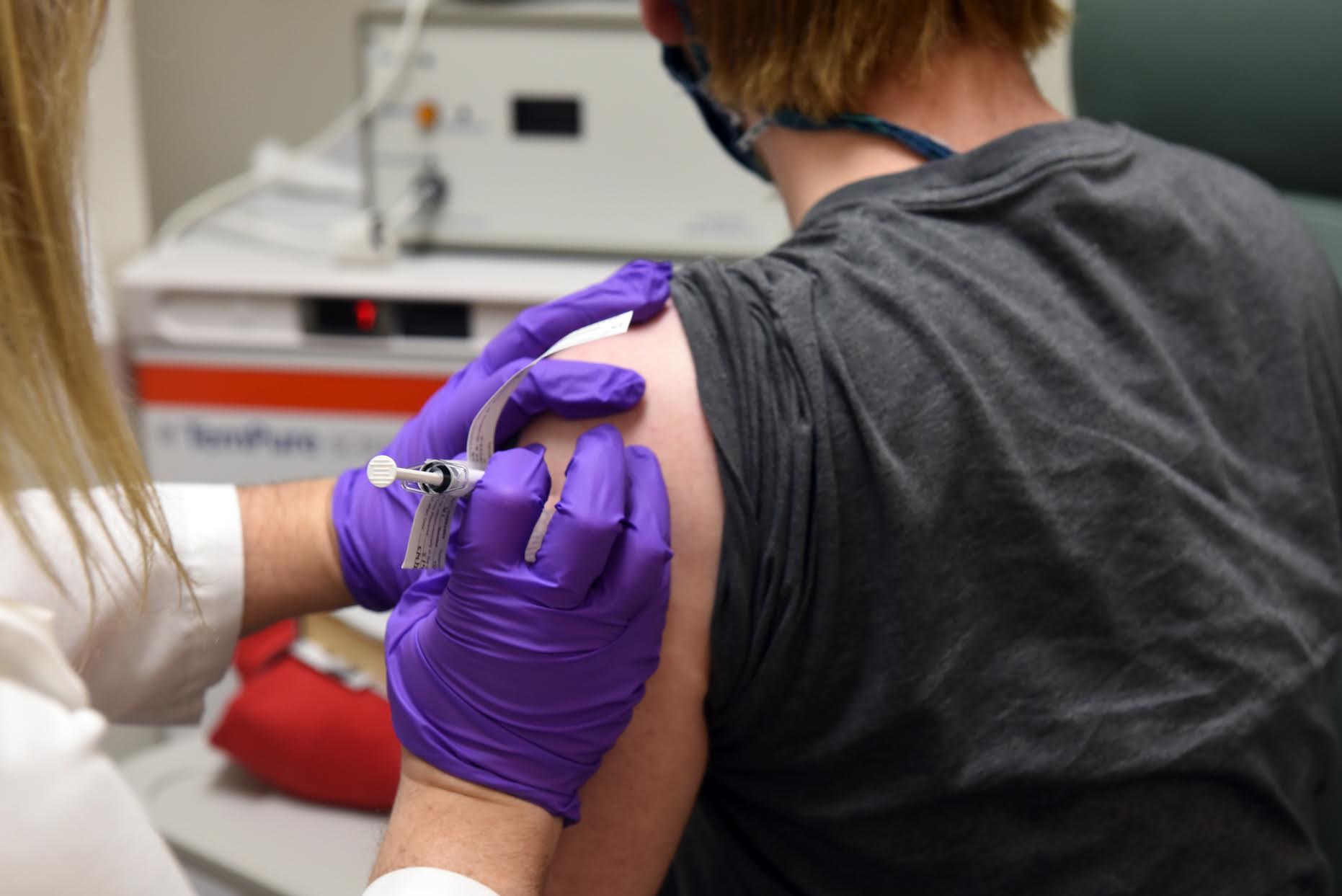
Acuerdo permitirá el suministro de un millón de dosis de la vacuna candidata desarrollada junto con la Universidad de Oxford y AstraZeneca, a partir del primer trimestre de 2021.
Por EFE
AstraZeneca firmó un acuerdo con el Gobierno de Costa Rica para suministrar un millón de dosis de su vacuna candidata contra el COVID-19, AZD1222, desarrollada junto con la Universidad de Oxford. Se estima que la vacuna estará disponible a partir del primer trimestre del 2021, de resultar exitosos los ensayos clínicos en curso y sujeto a la aprobación de las agencias regulatorias.
AstraZeneca continúa avanzando en su respuesta para abordar los desafíos sin precedentes de la pandemia por COVID-19, al colaborar con distintos gobiernos y organizaciones multilaterales para lograr el objetivo de apoyar el acceso amplio y
equitativo de la vacuna AZD1222 a precio de costo durante la pandemia.
Rafael Mendoza, Presidente de AstraZeneca para la región de Centroamérica y Caribe, señaló: “En AstraZeneca reafirmamos nuestro compromiso de impulsar un acceso amplio y equitativo de la vacuna candidata AZD1222 en Centroamérica y Caribe, en caso de que resulte segura y eficaz. Nos sentimos honrados que el Gobierno de Costa Rica haya elegido a la vacuna candidata AZD1222 como parte de su plan de vacunación contra el COVID-19 y seguiremos colaborando para co-crear soluciones y responder a los múltiples desafíos de esta pandemia”.
Los ensayos clínicos Fase II/III están desarrollándose en Reino Unido, Estados Unidos y Brasil, mientras que los ensayos clínicos Fase I/II están en curso en Sudáfrica, Japón, Kenia y Rusia. Estos ensayos determinarán la protección de la vacuna contra el COVID-19 y medirán la seguridad y respuesta inmunológica en hasta 50.000 participantes a nivel mundial de un amplio rango de edad y diversos grupos y geografías.
El primero de octubre, la Agencia Europea de Medicamentos (EMA) anunció que su Comité de Medicamentos de Uso Humano (CHMP) había iniciado un proceso de revisión continua de AZD1222. El proceso de revisión continua es una herramienta regulatoria flexible que utilizan los reguladores para avanzar en la evaluación de un medicamento o una vacuna prometedores durante una emergencia de salud pública. AZD1222 fue la primera vacuna COVID-19 que es aceptada para este proceso por la EMA.
Otras agencias regulatorias, incluyendo las de Canadá, Japón, Brasil, México, Chile, Australia, Corea del Sur y Suiza también han iniciado protocolos de revisión para la vacuna candidata.